冰合试剂 · 2026-04-15 · 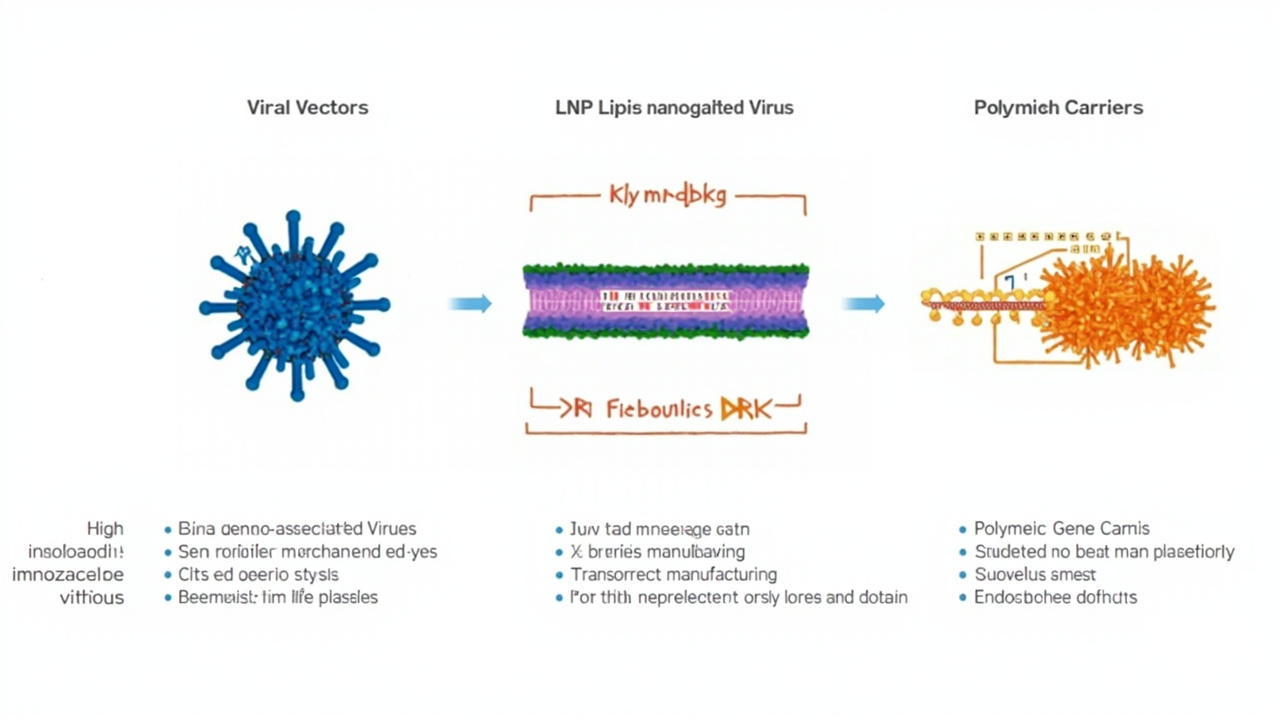
基因递送三大平台技术对比:病毒载体(AAV)vs LNP脂质纳米颗粒 vs 聚合物载体
基因治疗的核心挑战不在于目标基因的序列设计,而在于如何将这些遗传物质(DNA质粒、mRNA、siRNA或基因编辑工具)安全有效地送达目标细胞内部。核酸分子外排于细胞膜(由磷酸骨架携带负电荷且分子量极大),无法以自由扩散方式进入细胞。因此,基因递送载体(Gene Delivery Vector)成为决定基因治疗成败的核心技术瓶颈。
截至2026年初,全球已批准的基因治疗产品超过50款(涵盖体内基因治疗、体外CAR-T及RNAi疗法),而处于临床在研阶段的基因疗法管线更超过7000个(据医药魔方CGT管线追踪数据)。在这背后,两大类递送技术——病毒载体和非病毒载体——各有优劣,相互补充,共同推动基因治疗走向临床。
病毒在数亿年进化中发展出了精确入侵特定宿主细胞的能力,基因治疗正是借用了这一天然机制。常用的病毒载体包括腺相关病毒(AAV)、慢病毒(LV)和腺病毒(AdV),其中AAV因免疫原性低、可感染分裂与非分裂细胞、长期表达等优势,成为体内基因治疗的主流载体。
腺相关病毒(AAV)的优势:安全性良好(FDA已批准Luxturna、Zolgensma等AAV产品);可实现长期稳定表达(部分临床数据显示AAV载体可在体内存续超过5年);血清型丰富(AAV1-AAV9等不同亚型对不同组织有不同靶向性);宿主基因组整合风险低(相对于慢病毒)。
AAV的核心局限:包装容量受限(通常不超过4.7 kb基因组),无法递送大片段基因(如dystrophin基因,全长约11 kb无法装入AAV);大量重复给药可能触发免疫中和抗体;生产工艺复杂、规模化难度大、成本高。
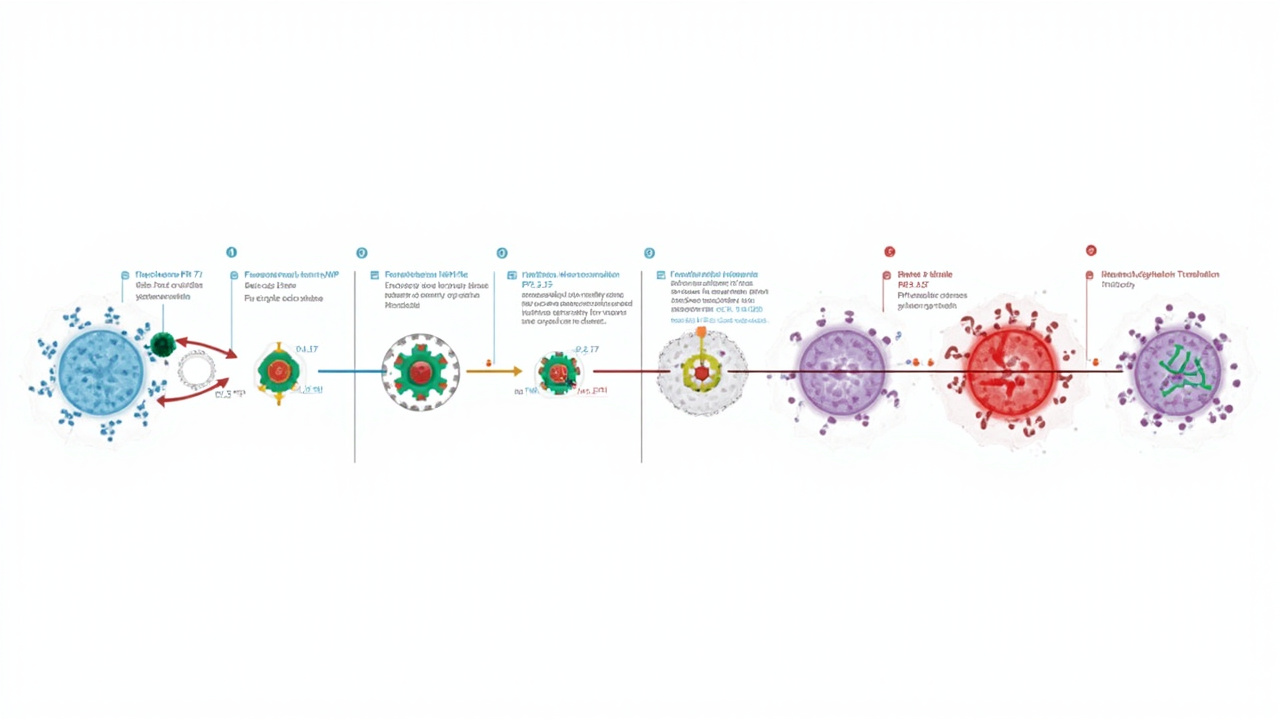
mRNA-LNP脂质纳米颗粒细胞内递送五步路径:血液循环→细胞内吞→内涵体积累→内涵体逃逸→胞质蛋白翻译
非病毒载体以物理或化学方式介导核酸的细胞内递送,不依赖病毒天然感染机制。其中,LNP(脂质纳米颗粒)因2018年以来COVID-19 mRNA疫苗的巨大成功(Pfizer/BioNTech的BNT162b2、Moderna的mRNA-1273)已成为非病毒递送领域最成熟、临床应用最广泛的技术平台。
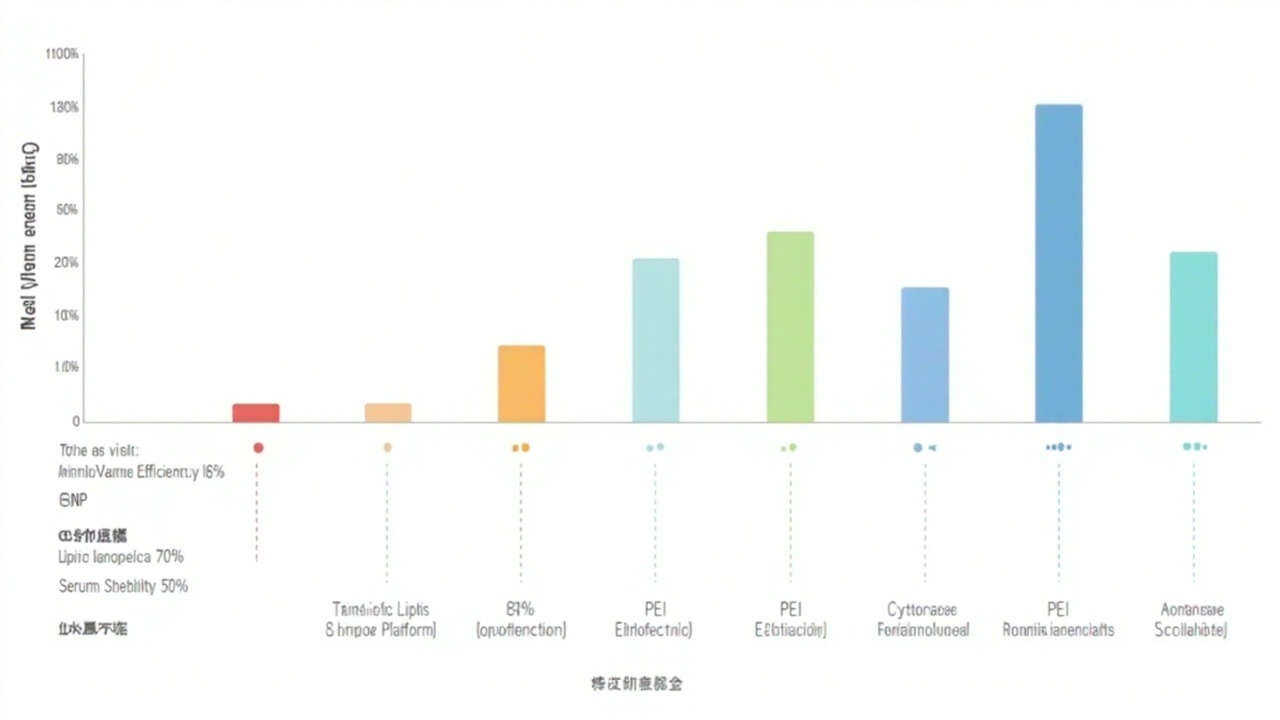
主要非病毒基因递送系统性能对比:转染效率、细胞毒性、血清稳定性、生产可放大性
LNP-mRNA疫苗在COVID-19疫情防控中展现了超过94%的保护率(Pfizer/BioNTech III期临床数据,2020年),核心在于LNP将mRNA安全送达细胞质的能力。LNP由四大组分构成:可电离脂质(50 mol%,负责mRNA包封与内涵体逃逸)、DSPC磷脂(10 mol%,结构稳定)、胆固醇(38.5 mol%,调节膜流动性)、PEG-脂质(1.5 mol%,减少蛋白吸附延长循环)。在中性血液环境中,可电离脂质呈电中性,mRNA被牢牢包裹在LNP内部疏水核心中;进入细胞后,酸性内涵体环境触发脂质质子化,引发膜融合与mRNA释放。
聚乙烯亚胺(PEI)是基因递送中最经典的阳离子聚合物,其分子链上的伯胺/仲胺基团质子化后携带正电荷,可通过静电吸引与带负电的核酸分子形成纳米级复合物(polyplex)。然而,传统线性PEI(25 kDa)的细胞毒性是主要瓶颈——高密度正电荷与细胞膜发生非特异性相互作用,引发膜破裂和细胞凋亡。超支化聚乙烯亚胺(bPEI)和聚β-氨基酯(PBAE)的开发部分改善了这一问题,但临床转化仍受限于安全性数据不足。
冰合试剂布局:聚氨基酸载体(如聚赖氨酸PLL、聚精氨酸PEI替代物)作为新一代可生物降解聚合物,具有细胞毒性低、内涵体逃逸效率高的优势,可通过定制合成特定聚合度和功能末端,满足不同基因递送场景的需求。
| 产品名称 | 递送技术 | 适应症 | 年份 | 研发企业 |
|---|---|---|---|---|
| Luxturna(voretigene neparvovec) | AAV2载体(体内) | 遗传性视网膜营养不良症(Leber先天性黑矇) | 2017 | Spark Therapeutics |
| Zolgensma(onasemnogene abeparvovec) | AAV9载体(体内) | 脊髓性肌萎缩症(SMA)1型 | 2019 | Novartis |
| BNT162b2(复必泰) | LNP-mRNA(体内) | 预防性COVID-19 mRNA疫苗 | 2020 | Pfizer/BioNTech |
| mRNA-1273(Spikevax) | LNP-mRNA(体内) | 预防性COVID-19 mRNA疫苗 | 2021 | Moderna |
| Onpattro(patisiran) | LNP-siRNA(体内) | 转甲状腺素蛋白淀粉样变性(hATTR) | 2018 | Alnylam |
| Yescarta(axicabtagene ciloleucel) | 慢病毒载体(体外CAR-T) | 复发/难治性大B细胞淋巴瘤 | 2017 | Kite Pharma |
* 上表为部分代表性上市品种;数据来源:FDA审批文件、EMA审评报告、Alnylam/Pfizer/Moderna/Novartis公开披露(2020-2025年);临床疗效数据来自企业关键性注册临床试验(已发表于NEJM/Lancet)
据医药魔方Pharmcube《下一代创新药全球研发趋势分析》(2025年),中国在全球细胞与基因治疗(CGT)研发管线中已占据领先地位,在研CAR-T产品946个(全球第一),基因疗法临床试验数量于2024年首次超越国外(中国111 vs 国外87)。以传奇生物、药明巨诺、科济药业为代表的CAR-T企业已有多款产品获批上市;以信念医药、朗昇生物为代表的基因治疗企业也在AAV基因治疗领域取得突破进展。
冰合试剂可提供基因递送研发所需的核心脂质与聚合物原料,支持LNP-mRNA、聚合物基因载体及AAV生产辅助试剂的科研需求:
| 产品类别 | 典型产品 | 官网链接 |
|---|---|---|
| LNP核心脂质(可电离脂质) | MC3 (DLin-MC3-DMA)、DODMA、306-O13B等 | LZ01 可电离脂质系列 |
| LNP磷脂结构组分 | DSPC、DPPC、DOPE、DMPC、胆固醇等 | LZ 磷脂系列产品 |
| LNP PEG脂质(隐身层) | DMG-PEG2000、DSPE-PEG2000、DSPE-PEG5000等 | JY PEG修饰剂系列 |
| 功能化磷脂(靶向修饰) | DSPE-PEG-NH2、DSPE-PEG-Mal、DSPE-PEG-COOH等 | LZ05 功能化磷脂系列 |
| 点击化学(基因载体功能化) | DBCO-NHS、DBCO-Maleimide、TCO-NHS等 | DJ01 点击化学DBCO系列 |
| 聚氨基酸载体(聚合物基因载体) | 聚赖氨酸盐酸盐(PLL)、聚精氨酸(R8)等 | JHLL 聚氨基酸聚合物系列 |
参考文献来源说明:本文数据综合整理自医药魔方Pharmcube《下一代创新药全球研发趋势分析》(2025年)、FDA审批文件(Luxturna/Zolgensma/Onpattro)、Pfizer-BioNTech和Moderna公开披露的BNT162b2及mRNA-1273 III期临床数据(NEJM 2020-2021)、Alnylam Onpattro临床数据(Lancet 2018)、Cortellis数据库(全球CGT在研管线统计,2026年1月更新)。中国CGT临床试验数据来自国家药品监督管理局药品审评中心(CDE)公开登记信息。
温馨提示:本文内容仅供科研参考,不构成临床或用药建议。冰合试剂可提供基因递送研究所需的LNP脂质、PEG修饰剂及功能化磷脂,批次间一致性好,适合科研用户进行基因递送载体构建与早期工艺开发研究。